Zjawisko zamiany energii chemicznej, uwalnianej podczas reakcji chemicznych, na energię świetlną nazywamy chemiluminescencją.
Należy podkreślić, że wbrew obiegowej opinii nie wszystkie związki fosforu świecą, i nie wszystkie substancje świecące zawierają fosfor.

Opis eksperymentu (wersja 1):
Wyjaśnienie:
Biały fosfor jest jedną z form (alotropów) fosforu. Ma postać białego, miękkiego (daje się kroić nożem), niskotopliwego (t.t. 44°C), woskowatego ciała stałego. Atomy fosforu tworzą cząsteczki P4 o budowie tetraedrycznej.
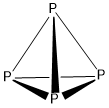

Biały fosfor jest bardzo reaktywny – w kontakcie z powietrzem ulega utlenianiu. Produktami tej reakcji jest tlenek fosforu(III), P4O6 i tlenek fosforu(V), P4O10. Procesowi utleniania towarzyszy emisja światła (chemiluminescencja).
Mechanizm chemiluminescencji białego fosforu ma złożoną naturę. Jej zrozumienie wymagało wielu badań, które przyniosły kilka interesujących obserwacji, m.in.:
- światło emitowane podczas utleniania P4 składa się z kilku komponentów o różnych długościach fali (różnej barwie) – od zakresu ultrafioletu do podczerwieni;
- przy dużym stężeniu tlenu chemiluminescencja nie występuje;
- do wystąpienia chemiluminescencji niezbędne jest para wodna, a emitowane światło różni się przy użyciu wody ciężkiej (D2O) zamiast zwykłej (H2O);
Ustalono, że głównym źródłem światła powstającego podczas utleniania P4 jest ekscymer (PO)2*. Ekscymer to układ molekularny (kompleks) złożony z dwóch cząsteczek, z których jedna jest wzbudzona (posiada nadmiar energii), a druga nie – w tym wypadku ekscymer zbudowany jest z cząsteczki PO i jej wzbudzonej formy, PO*. Reakcji rozpadu ekscymeru towarzyszy oddanie nadmiaru energii i emisja światła w szerokim zakresie długości fal, 350-800 nm, z maksimum około 520 nm (barwa niebieskawozielona):
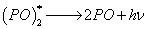
Wzbudzone cząsteczki HPO odpowiadają z kolei za emisję światła w postaci kilku pasm o niewielkim zakresie długości fali około 525 nm:

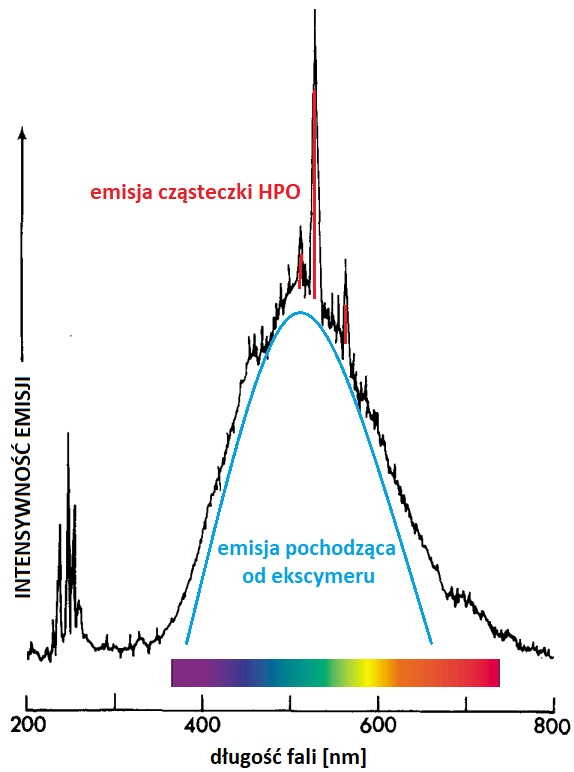
Wydajność kwantowa reakcji jest bardzo mała – szacuje się, że na 2000 utlenionych cząsteczek P4 powstaje jeden foton.
Za odkrywcę białego fosforu uważa się Henniga Brandta, niemieckiego alchemika, który podczas prażenia z piaskiem osadu powstałego po odparowaniu moczu (ok. 50 L) uzyskał świecącą w ciemności substancję (1669 r.). Wizję artystyczną tego odkrycia przedstawił Joseph Wright of Derby (link). Wiele wskazuje jednak na to, że odkrycie fosforu miało miejsce ponad 100 lat wcześniej – Paracelsus w swoich pismach donosi o otrzymaniu „sopelków” i „elementów ognia” podczas prażenia moczu.
Do poczytania dla zainteresowanych:
(i) E.N. Harvey; A history of luminescence. From the earliest times until 1900. Dover Publications Inc., New York, 2005.
(ii) A.E. Wait (ed.); The hermetic and alchemical writings of the Aureolus Philippus Theophrastus Bombast, of Hohenheim, called Paracelsus the Great, Vol. II. James Elliott and Co., London, 1894.
(iii) B.P. Davies, B.A. Thrus; The reactions of atomic oxygen with phosphorus and with phosphine. Proc. Royal Soc. A, 302: 243-252, 1968. DOI: 10.1098/rspa.1968.0007
(iv) R.J. Van Zee, A.U. Khan; A Striking Deuterium Effect in Phosphorus Chemiluminescence. Identification of the Emitting Species. J. Am. Chem. Soc., 96(21): 6805-6806, 1974. DOI: 10.1021/ja00828a067
(v) R.J. VanZee, A.U. Khan; The electronic origin of the cool green phosphorus flame. Chem. Phys. Lett., 36(1): 123-125, 1975. DOI: 10.1016/0009-2614(75)85703-4
(vi) R.J. VanZee, A.U. Khan; Infrared emission from ultraviolet and vacuum ultraviolet states of PO in the cool phosphorus chemiluminescence flame. Chem. Phys. Lett., 41(1): 180-182, 1976. DOI: 10.1016/0009-2614(76)85278-5
(vii) R.J. VanZee, A.U. Khan; Transient emitting species in phosphorus chemiluminescence. J. Chem. Phys., 65: 1764-1772, 1976. DOI:10.1063/1.433322
(viii) P.A. Hamilton, T.P. Murrells; Mechanism for the chemiluminescence in oxygen-phosphorus systems. J. Phys. Chem., 90(1): 182-185, 1986. DOI:10.1021/j100273a041
(ix) R.J. VanZee, A.U. Khan; The phosphorescence of phosphorus. J. Phys. Chem., 80(20): 2240-2242, 1976. DOI: 10.1021/j100561a021


Komentarze